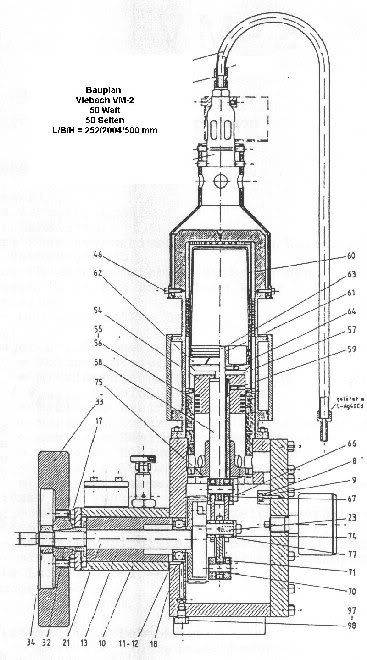
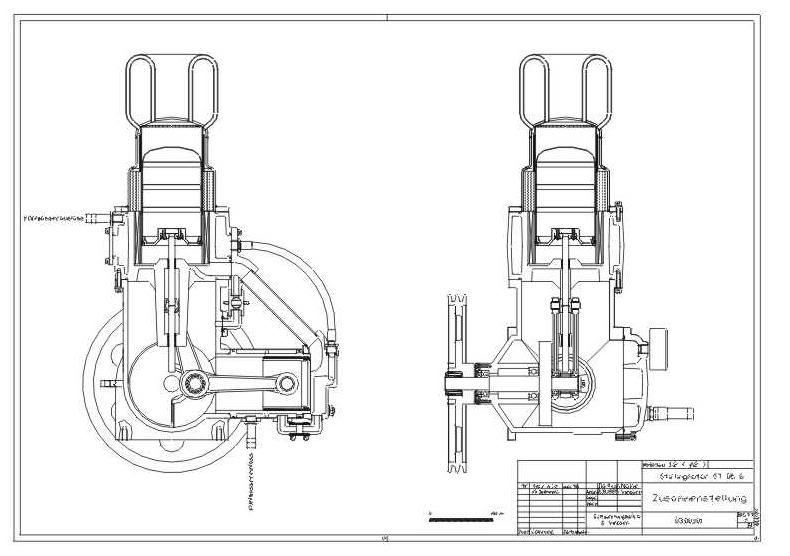
Salve a tutti, sono nuovo, mi chiamo Dino e ho 27 anni, seguo da molto tempo questo forum e adesso vorrei cimentarmi nella costruzione di un motore a combustione esterna, non so ancora se Stirling, Rankine o altro, per i macchinari necessari alle lavorazioni nessun problema, mio padre è meccanico ed io programmo macchine CNC, ma avrei qualche dubbio sui calcoli da fare per evitare di perdere tempo e soldi.
Vorrei sapere con che delta di temperatura l' aria raddoppia la sua pressione in modo da poter calcolare la sezione e la corsa dei cilindri in base alla temperatura disponibile.
Grazie mille
Dino
Vorrei sapere con che delta di temperatura l' aria raddoppia la sua pressione in modo da poter calcolare la sezione e la corsa dei cilindri in base alla temperatura disponibile.
Grazie mille
Dino